Patente do Ozempic expira, mas versões mais baratas ainda não chegaram às farmácias
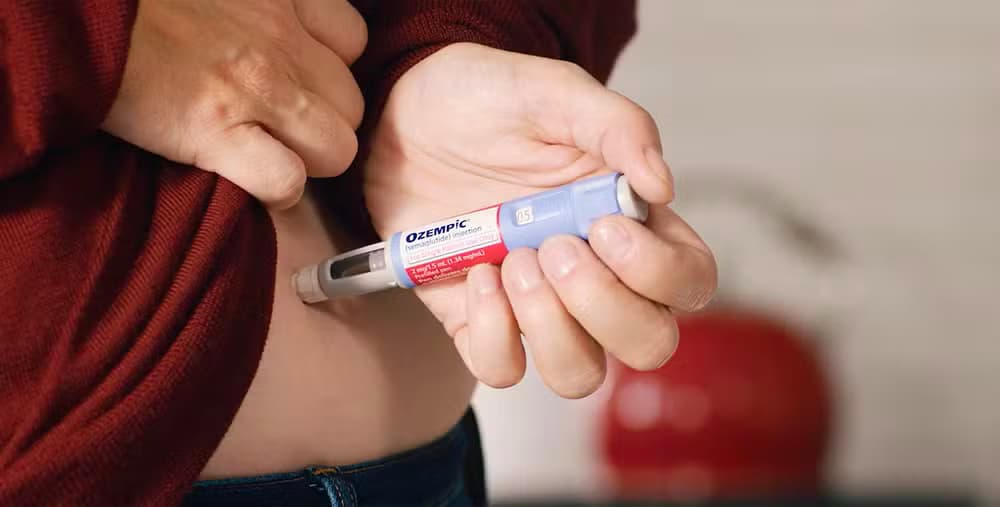
Nesta sexta-feira (20/3), expirou a patente da semaglutida, substância ativa de medicamentos como o Ozempic e o Wegovy, utilizados para o tratamento de diabetes tipo 2 e obesidade. A exclusividade da dinamarquesa Novo Nordisk sobre o princípio ativo, que durava 20 anos, chegou ao fim, abrindo caminho para que outras farmacêuticas possam produzir e comercializar versões próprias do medicamento no Brasil.
A expectativa era de que a queda da patente resultasse imediatamente em opções mais acessíveis nas prateleiras das farmácias, reduzindo o custo atual de uma caneta, que hoje custa, em média, R$ 1 mil, dependendo da dosagem. No entanto, devido a uma série de fatores técnicos e regulatórios, esse movimento ainda não ocorreu.
Atualmente, há 15 pedidos nacionais de medicamentos à base de semaglutida em análise pela Agência Nacional de Vigilância Sanitária (Anvisa), mas nenhum foi aprovado até o momento.
Por que a chegada dos genéricos demora?
Diferentemente de medicamentos mais simples, como a dipirona, que possuem uma composição química bem definida, a semaglutida é uma molécula complexa. Classificada como um peptídeo, ela fica na fronteira entre o sintético e o biológico, o que exige uma análise técnica mais rigorosa por parte da agência reguladora.
Segundo especialistas, esse tipo de substância pode ser produzida por diferentes métodos, o que impacta diretamente a regulação. O Brasil ainda não contava com uma norma consolidada para esse tipo de medicamento, que não se encaixa nas categorias tradicionais. Por isso, a Anvisa precisa avaliar cada pedido com base em critérios técnicos específicos e referências internacionais, tornando o processo mais detalhado e demorado.
Os primeiros pedidos começaram a ser feitos em 2023. Desde então, a agência analisa cada processo individualmente.
Leia mais
Mercado de canetas emagrecedoras deve crescer com fim da exclusividade de patente
Ozempic e Mounjaro vendidos ilegalmente entram na mira do MPAM
Pedidos em andamento
Atualmente, o cenário dos pedidos nacionais é o seguinte:
Dois medicamentos (das farmacêuticas EMS e Ávita Care) estão em fase de cumprimento de exigências: a Anvisa solicitou esclarecimentos no início de março, e as empresas têm até 120 dias para responder;
Cinco pedidos estão em análise e devem ter uma primeira decisão, que pode ser a solicitação de mais esclarecimentos, ainda no primeiro semestre deste ano;
Outros nove pedidos ainda não tiveram a análise iniciada.
As propostas mais avançadas são justamente as da EMS e da Ávita Care, que fizeram investimentos bilionários para entrar nesse mercado. A EMS, por exemplo, investiu R$ 1,2 bilhão na produção nacional da semaglutida, com a expansão de uma planta em Hortolândia (SP). A empresa afirma que a unidade terá capacidade para produzir até 20 milhões de canetas por ano.
A Anvisa informou que solicitou esclarecimentos às duas empresas na fase mais avançada no início de março. Se os dados apresentados forem considerados suficientes, os produtos podem ser aprovados. Por isso, a expectativa é que ao menos uma dessas versões chegue às farmácias até junho.
Impacto nos preços
A queda da patente deve impactar os preços dos medicamentos à base de semaglutida, mas esse efeito não será visto de forma imediata. A diminuição dos valores depende da entrada efetiva de concorrentes no mercado, o que ainda não aconteceu no Brasil. Mesmo assim, com o aumento da concorrência ao longo do tempo, a tendência é que os preços sejam pressionados para baixo.
A Novo Nordisk, detentora da patente original, tentou estender a exclusividade por mais 12 anos na Justiça, mas perdeu a disputa.





